摘要:針對HER2低表達(dá)(IHC 1+或IHC 2+/ISH-)轉(zhuǎn)移性乳腺癌化療后治療困境,研究人員開展III期DESTINY-Breast04試驗(yàn)。
在乳腺癌精準(zhǔn)治療領(lǐng)域,人類表皮生長因子受體2(HER2)表達(dá)狀態(tài)長期主導(dǎo)著治療決策格局。傳統(tǒng)上,HER2陽性(免疫組化[IHC] 3+或IHC 2+/原位雜交[ISH]+)患者可從HER2靶向治療中獲益,而HER2陰性(IHC 0、IHC 1+或IHC 2+/ISH-)患者則缺乏有效的靶向治療選擇。然而,隨著檢測技術(shù)的精進(jìn)和新型抗體藥物偶聯(lián)物(ADC)的出現(xiàn),HER2低表達(dá)(IHC 1+或IHC 2+/ISH-)這一新分類逐漸受到關(guān)注?;仡櫺匝芯匡@示,約65%原屬HER2陰性的腫瘤實(shí)際上符合HER2低表達(dá)標(biāo)準(zhǔn),這為大量患者提供了新的治療機(jī)會。
激素受體(HR)狀態(tài)同樣是影響乳腺癌預(yù)后的關(guān)鍵因素。根據(jù)美國臨床腫瘤學(xué)會/美國病理學(xué)家學(xué)院(ASCO/CAP)指南,HR陽性定義為≥1%腫瘤細(xì)胞核表達(dá)雌激素受體(ER)或孕激素受體(PR)。值得注意的是,ER低陽性(1%-10%染色)患者對內(nèi)分泌治療反應(yīng)不佳,其臨床特征更接近HR陰性腫瘤,這增加了治療選擇的復(fù)雜性。

圖1 德曲妥珠單抗在HER2低表達(dá)轉(zhuǎn)移性乳腺癌中的應(yīng)用:隨機(jī)三期DESTINY-Breast04試驗(yàn)的長期生存分析
DESTINY-Breast04試驗(yàn)應(yīng)運(yùn)而生,旨在解決HER2低表達(dá)轉(zhuǎn)移性乳腺癌患者化療后的治療難題。這項(xiàng)開放標(biāo)簽、隨機(jī)、III期臨床研究比較了Trastuzumab deruxtecan(T-DXd)與醫(yī)生選擇的化療(TPC)在既往接受過1-2線化療的HER2低表達(dá)轉(zhuǎn)移性乳腺癌患者中的療效和安全性。T-DXd是一種由人源化抗HER2單克隆抗體與拓?fù)洚悩?gòu)酶I抑制劑通過可裂解連接子組成的ADC,具有獨(dú)特的"旁觀者效應(yīng)",可殺傷鄰近腫瘤細(xì)胞。
主要技術(shù)方法包括:采用中心實(shí)驗(yàn)室驗(yàn)證的VENTANA HER2/neu(4B5)檢測進(jìn)行免疫組化分析,ISH檢測使用INFORM HER2 Dual ISH DNA Probe Cocktail assay;通過盲態(tài)獨(dú)立中心審查(BICR)和研究者評估評估療效終點(diǎn);安全性評估遵循MedDRA和CTCAE標(biāo)準(zhǔn);獨(dú)立裁定委員會對間質(zhì)性肺病/肺炎病例進(jìn)行專門評估。研究納入577例經(jīng)中心實(shí)驗(yàn)室確認(rèn)的HER2低表達(dá)轉(zhuǎn)移性乳腺癌患者。
療效結(jié)果
在延長至32.0個月的中位隨訪后,T-DXd顯示出持續(xù)的生存優(yōu)勢??傮w人群中,T-DXd組中位總生存期(OS)為22.9個月,顯著優(yōu)于TPC組的16.8個月(風(fēng)險比[HR] 0.69)。HR陽性隊(duì)列中,T-DXd組中位OS為23.9個月,TPC組為17.6個月(HR 0.69)。甚至在探索性分析的HR陰性隊(duì)列中,T-DXd組中位OS達(dá)17.1個月,而TPC組僅8.3個月(HR 0.58),24個月OS率更是TPC組的近三倍(32.6% vs 11.8%)。
無進(jìn)展生存期方面,研究者評估的總體人群中位PFS在T-DXd組為8.8個月,TPC組為4.2個月(HR 0.36)。HR陽性隊(duì)列中,T-DXd組中位PFS為9.6個月,TPC組為4.2個月(HR 0.37)。HR陰性隊(duì)列同樣顯示T-DXd優(yōu)勢(6.3 vs 2.9個月;HR 0.29)。
探索性分析揭示了不同ER表達(dá)水平患者的獲益情況。在ER>10%亞組中,T-DXd組中位OS為24.0個月,TPC組為18.9個月(HR 0.72);ER低陽性(1%-10%)亞組中,T-DXd組中位OS達(dá)22.3個月,而TPC組僅10.2個月(HR 0.40),表明T-DXd療效不受ER表達(dá)水平影響。
安全性特征
T-DXd安全性特征與初步分析一致,未出現(xiàn)新的安全性信號。中位治療持續(xù)時間T-DXd組為8.2個月,TPC組為3.5個月。經(jīng)暴露校正后,T-DXd組任何級別治療相關(guān)不良事件(TEAEs)發(fā)生率為1.16/患者年,低于TPC組的2.64/患者年。
T-DXd組最常見任何級別藥物相關(guān)TEAEs包括惡心(76.0%)、疲勞(55.0%)、嘔吐(40.7%)和脫發(fā)(39.9%)?!?級藥物相關(guān)TEAEs主要為中性粒細(xì)胞減少(14.6%)、貧血(10.8%)和疲勞(9.7%)。
特別關(guān)注的不良事件中,經(jīng)裁定的藥物相關(guān)間質(zhì)性肺病(ILD)/肺炎發(fā)生率為12.1%,多數(shù)為低級事件(1-2級占10%),≥3級事件占2.2%。左心室功能障礙發(fā)生率為5.1%,主要為射血分?jǐn)?shù)下降(4.9%),無4級事件。
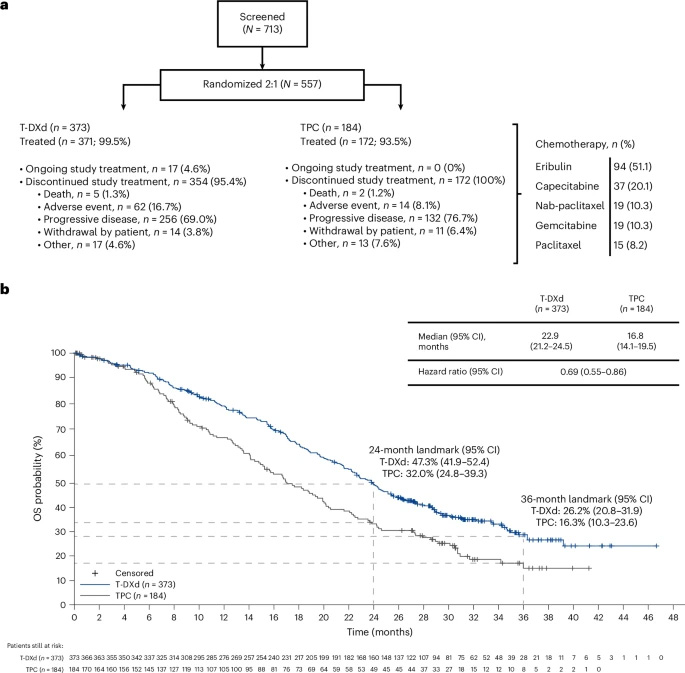
圖2 患者分組情況及總?cè)巳嚎偵嫫诘腒aplan–Meier分析曲線
研究結(jié)論與意義
DESTINY-Breast04的最終分析證實(shí)了T-DXd在HER2低表達(dá)轉(zhuǎn)移性乳腺癌中的持久臨床獲益。無論HR狀態(tài)如何,T-DXd相比化療顯著改善生存結(jié)局,且安全性可控。該研究不僅確立了T-DXd作為HER2低表達(dá)乳腺癌化療后標(biāo)準(zhǔn)治療的地位,更重新定義了乳腺癌分子分型格局。
值得注意的是,HER2低表達(dá)和最新提出的HER2超低表達(dá)(IHC 0伴微弱染色)的識別仍是臨床挑戰(zhàn)。隨著DESTINY-Breast06試驗(yàn)證實(shí)T-DXd在HER2超低表達(dá)患者中的療效,優(yōu)化檢測方法和統(tǒng)一病理判讀標(biāo)準(zhǔn)顯得尤為重要。這項(xiàng)發(fā)表在《Nature Medicine》的研究標(biāo)志著乳腺癌靶向治療進(jìn)入新紀(jì)元,為傳統(tǒng)認(rèn)為"不可靶向"的患者群體帶來了希望,推動了精準(zhǔn)醫(yī)療理念的深化和實(shí)踐的拓展。
研究的局限性包括開放標(biāo)簽設(shè)計(jì)可能引入偏倚,且探索性分析樣本量有限。未來研究應(yīng)聚焦生物標(biāo)志物開發(fā)、耐藥機(jī)制探索以及T-DXd在更早線治療中的應(yīng)用,進(jìn)一步優(yōu)化HER2低表達(dá)乳腺癌的治療策略。
參考資料
[1] Trastuzumab deruxtecan in HER2-low metastatic breast cancer: long-term survival analysis of the randomized, phase 3 DESTINY-Breast04 trial
摘要:針對HER2低表達(dá)(IHC 1+或IHC 2+/ISH-)轉(zhuǎn)移性乳腺癌化療后治療困境,研究人員開展III期DESTINY-Breast04試驗(yàn)。
在乳腺癌精準(zhǔn)治療領(lǐng)域,人類表皮生長因子受體2(HER2)表達(dá)狀態(tài)長期主導(dǎo)著治療決策格局。傳統(tǒng)上,HER2陽性(免疫組化[IHC] 3+或IHC 2+/原位雜交[ISH]+)患者可從HER2靶向治療中獲益,而HER2陰性(IHC 0、IHC 1+或IHC 2+/ISH-)患者則缺乏有效的靶向治療選擇。然而,隨著檢測技術(shù)的精進(jìn)和新型抗體藥物偶聯(lián)物(ADC)的出現(xiàn),HER2低表達(dá)(IHC 1+或IHC 2+/ISH-)這一新分類逐漸受到關(guān)注?;仡櫺匝芯匡@示,約65%原屬HER2陰性的腫瘤實(shí)際上符合HER2低表達(dá)標(biāo)準(zhǔn),這為大量患者提供了新的治療機(jī)會。
激素受體(HR)狀態(tài)同樣是影響乳腺癌預(yù)后的關(guān)鍵因素。根據(jù)美國臨床腫瘤學(xué)會/美國病理學(xué)家學(xué)院(ASCO/CAP)指南,HR陽性定義為≥1%腫瘤細(xì)胞核表達(dá)雌激素受體(ER)或孕激素受體(PR)。值得注意的是,ER低陽性(1%-10%染色)患者對內(nèi)分泌治療反應(yīng)不佳,其臨床特征更接近HR陰性腫瘤,這增加了治療選擇的復(fù)雜性。

圖1 德曲妥珠單抗在HER2低表達(dá)轉(zhuǎn)移性乳腺癌中的應(yīng)用:隨機(jī)三期DESTINY-Breast04試驗(yàn)的長期生存分析
DESTINY-Breast04試驗(yàn)應(yīng)運(yùn)而生,旨在解決HER2低表達(dá)轉(zhuǎn)移性乳腺癌患者化療后的治療難題。這項(xiàng)開放標(biāo)簽、隨機(jī)、III期臨床研究比較了Trastuzumab deruxtecan(T-DXd)與醫(yī)生選擇的化療(TPC)在既往接受過1-2線化療的HER2低表達(dá)轉(zhuǎn)移性乳腺癌患者中的療效和安全性。T-DXd是一種由人源化抗HER2單克隆抗體與拓?fù)洚悩?gòu)酶I抑制劑通過可裂解連接子組成的ADC,具有獨(dú)特的"旁觀者效應(yīng)",可殺傷鄰近腫瘤細(xì)胞。
主要技術(shù)方法包括:采用中心實(shí)驗(yàn)室驗(yàn)證的VENTANA HER2/neu(4B5)檢測進(jìn)行免疫組化分析,ISH檢測使用INFORM HER2 Dual ISH DNA Probe Cocktail assay;通過盲態(tài)獨(dú)立中心審查(BICR)和研究者評估評估療效終點(diǎn);安全性評估遵循MedDRA和CTCAE標(biāo)準(zhǔn);獨(dú)立裁定委員會對間質(zhì)性肺病/肺炎病例進(jìn)行專門評估。研究納入577例經(jīng)中心實(shí)驗(yàn)室確認(rèn)的HER2低表達(dá)轉(zhuǎn)移性乳腺癌患者。
療效結(jié)果
在延長至32.0個月的中位隨訪后,T-DXd顯示出持續(xù)的生存優(yōu)勢。總體人群中,T-DXd組中位總生存期(OS)為22.9個月,顯著優(yōu)于TPC組的16.8個月(風(fēng)險比[HR] 0.69)。HR陽性隊(duì)列中,T-DXd組中位OS為23.9個月,TPC組為17.6個月(HR 0.69)。甚至在探索性分析的HR陰性隊(duì)列中,T-DXd組中位OS達(dá)17.1個月,而TPC組僅8.3個月(HR 0.58),24個月OS率更是TPC組的近三倍(32.6% vs 11.8%)。
無進(jìn)展生存期方面,研究者評估的總體人群中位PFS在T-DXd組為8.8個月,TPC組為4.2個月(HR 0.36)。HR陽性隊(duì)列中,T-DXd組中位PFS為9.6個月,TPC組為4.2個月(HR 0.37)。HR陰性隊(duì)列同樣顯示T-DXd優(yōu)勢(6.3 vs 2.9個月;HR 0.29)。
探索性分析揭示了不同ER表達(dá)水平患者的獲益情況。在ER>10%亞組中,T-DXd組中位OS為24.0個月,TPC組為18.9個月(HR 0.72);ER低陽性(1%-10%)亞組中,T-DXd組中位OS達(dá)22.3個月,而TPC組僅10.2個月(HR 0.40),表明T-DXd療效不受ER表達(dá)水平影響。
安全性特征
T-DXd安全性特征與初步分析一致,未出現(xiàn)新的安全性信號。中位治療持續(xù)時間T-DXd組為8.2個月,TPC組為3.5個月。經(jīng)暴露校正后,T-DXd組任何級別治療相關(guān)不良事件(TEAEs)發(fā)生率為1.16/患者年,低于TPC組的2.64/患者年。
T-DXd組最常見任何級別藥物相關(guān)TEAEs包括惡心(76.0%)、疲勞(55.0%)、嘔吐(40.7%)和脫發(fā)(39.9%)?!?級藥物相關(guān)TEAEs主要為中性粒細(xì)胞減少(14.6%)、貧血(10.8%)和疲勞(9.7%)。
特別關(guān)注的不良事件中,經(jīng)裁定的藥物相關(guān)間質(zhì)性肺病(ILD)/肺炎發(fā)生率為12.1%,多數(shù)為低級事件(1-2級占10%),≥3級事件占2.2%。左心室功能障礙發(fā)生率為5.1%,主要為射血分?jǐn)?shù)下降(4.9%),無4級事件。

圖2 患者分組情況及總?cè)巳嚎偵嫫诘腒aplan–Meier分析曲線
研究結(jié)論與意義
DESTINY-Breast04的最終分析證實(shí)了T-DXd在HER2低表達(dá)轉(zhuǎn)移性乳腺癌中的持久臨床獲益。無論HR狀態(tài)如何,T-DXd相比化療顯著改善生存結(jié)局,且安全性可控。該研究不僅確立了T-DXd作為HER2低表達(dá)乳腺癌化療后標(biāo)準(zhǔn)治療的地位,更重新定義了乳腺癌分子分型格局。
值得注意的是,HER2低表達(dá)和最新提出的HER2超低表達(dá)(IHC 0伴微弱染色)的識別仍是臨床挑戰(zhàn)。隨著DESTINY-Breast06試驗(yàn)證實(shí)T-DXd在HER2超低表達(dá)患者中的療效,優(yōu)化檢測方法和統(tǒng)一病理判讀標(biāo)準(zhǔn)顯得尤為重要。這項(xiàng)發(fā)表在《Nature Medicine》的研究標(biāo)志著乳腺癌靶向治療進(jìn)入新紀(jì)元,為傳統(tǒng)認(rèn)為"不可靶向"的患者群體帶來了希望,推動了精準(zhǔn)醫(yī)療理念的深化和實(shí)踐的拓展。
研究的局限性包括開放標(biāo)簽設(shè)計(jì)可能引入偏倚,且探索性分析樣本量有限。未來研究應(yīng)聚焦生物標(biāo)志物開發(fā)、耐藥機(jī)制探索以及T-DXd在更早線治療中的應(yīng)用,進(jìn)一步優(yōu)化HER2低表達(dá)乳腺癌的治療策略。
參考資料
[1] Trastuzumab deruxtecan in HER2-low metastatic breast cancer: long-term survival analysis of the randomized, phase 3 DESTINY-Breast04 trial



