摘要:研究描述了2000多種獲批藥物如何影響基因組編輯結果。
在一項新的研究中,萊比錫馬克斯普朗克進化人類學研究所的科學家分析了2000多種臨床批準的藥物對DNA修復和CRISPR基因組編輯結果的影響。他們發(fā)現(xiàn)了可用于改善基因組編輯的化合物,選擇性殺死培養(yǎng)癌細胞的分子,并進一步確定了兩種蛋白質在DNA修復中的新作用。
DNA雙鏈斷裂是基因組中至關重要的損傷,可以通過幾種方式修復。一些修復過程很快,在損傷部位引入額外的突變,而另一些修復過程需要更長的時間,但允許精確的糾正。這些途徑可以在基因組編輯中被利用,將突變引入人類細胞。這包括使用可編程的CRISPR-Cas基因剪刀在基因組的特定位置切割DNA。為了使細胞存活,細胞必須修復由此產生的斷裂,研究人員可以提供攜帶所需突變的DNA模板。這種突變結合的效率在很大程度上取決于修復途徑的活性,這就需要工具來抑制競爭途徑,以提高預期結果的效率。

圖1 將臨床安全藥物用于CRISPR基因編輯與合成致死性中的DNA修復通路選擇:一種老藥新用策略
馬克斯普朗克進化人類學研究所的一組科學家調查了fda批準的藥物對DNA修復途徑選擇的影響。該研究的主要作者之一Dominik Macak說:“隨著這些療法進入現(xiàn)實世界的臨床應用,了解日常藥物如何與基于crispr的治療相互作用將變得越來越重要?!彪S著首個CRISPR基因療法于2023年底在美國、英國和歐盟獲得批準,接受此類治療的患者可能還需要服用治療感染或慢性疾病的常見藥物。其中一些常規(guī)藥物會影響細胞過程,如DNA修復,進而影響治療的效果或安全性。
超過2000種藥物接受了測試
科學家們創(chuàng)建了一個全面的圖譜,展示了臨床批準的藥物如何影響人類細胞修復斷裂DNA的方式。他們測試了7000多種藥物條件,以確定每種化合物在靶向CRISPR切割后如何改變DNA修復的選擇。“我們預計該目錄將成為從事疾病建模、基因治療和腫瘤學工作的臨床醫(yī)生和研究人員的寶貴資源,”共同主要作者Philipp Kanis補充說。
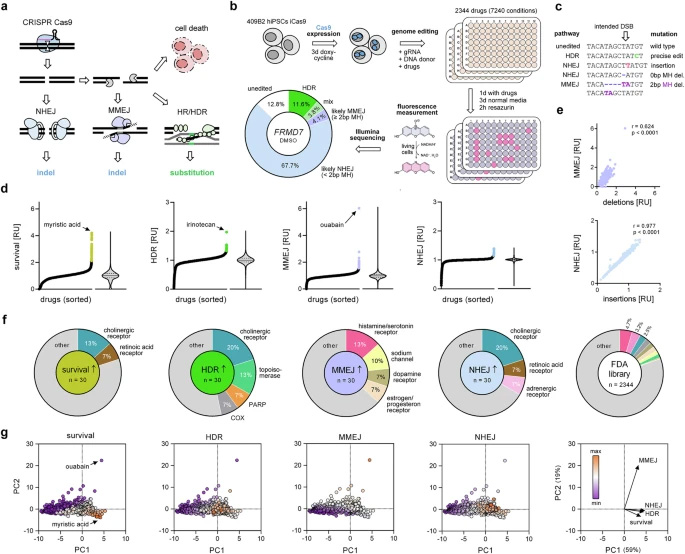
圖2 DNA雙鏈斷裂修復通路調控劑的藥物篩選
發(fā)現(xiàn)DNA修復調節(jié)中的新參與者
研究小組發(fā)現(xiàn)了幾種可以影響主要修復途徑的藥物。利用篩選數(shù)據(jù),他們進一步探索了以前未被認識到的對修復結果影響最大的藥物靶點。值得注意的是,他們發(fā)現(xiàn)了之前與基因組編輯無關的兩種蛋白質在DNA修復中的新作用。這些蛋白是雌激素受體2 (ESR2)和醛氧化酶1 (AOX1)。靶向抑制ESR2可以將精確編輯的效率提高多達四倍,而抑制AOX1的藥物可以用來殺死培養(yǎng)的癌細胞,這些癌細胞缺乏一種修復途徑——這種情況適用于許多癌細胞。
該項目的高級研究員Stephan Riesenberg說:“我們的研究確定了幾種被批準的藥物,作為治療dna修復缺陷癌癥的有希望的候選藥物,提供了目前治療方法之外的潛在選擇。”“然而,我們需要進一步的研究來驗證我們從培養(yǎng)細胞實驗中獲得的發(fā)現(xiàn)是否真的能轉化為現(xiàn)實世界的醫(yī)療用途?!?/div>
參考資料
[1] Repurposing clinically safe drugs for DNA repair pathway choice in CRISPR genome editing and synthetic lethality
摘要:研究描述了2000多種獲批藥物如何影響基因組編輯結果。
在一項新的研究中,萊比錫馬克斯普朗克進化人類學研究所的科學家分析了2000多種臨床批準的藥物對DNA修復和CRISPR基因組編輯結果的影響。他們發(fā)現(xiàn)了可用于改善基因組編輯的化合物,選擇性殺死培養(yǎng)癌細胞的分子,并進一步確定了兩種蛋白質在DNA修復中的新作用。
DNA雙鏈斷裂是基因組中至關重要的損傷,可以通過幾種方式修復。一些修復過程很快,在損傷部位引入額外的突變,而另一些修復過程需要更長的時間,但允許精確的糾正。這些途徑可以在基因組編輯中被利用,將突變引入人類細胞。這包括使用可編程的CRISPR-Cas基因剪刀在基因組的特定位置切割DNA。為了使細胞存活,細胞必須修復由此產生的斷裂,研究人員可以提供攜帶所需突變的DNA模板。這種突變結合的效率在很大程度上取決于修復途徑的活性,這就需要工具來抑制競爭途徑,以提高預期結果的效率。

圖1 將臨床安全藥物用于CRISPR基因編輯與合成致死性中的DNA修復通路選擇:一種老藥新用策略
馬克斯普朗克進化人類學研究所的一組科學家調查了fda批準的藥物對DNA修復途徑選擇的影響。該研究的主要作者之一Dominik Macak說:“隨著這些療法進入現(xiàn)實世界的臨床應用,了解日常藥物如何與基于crispr的治療相互作用將變得越來越重要?!彪S著首個CRISPR基因療法于2023年底在美國、英國和歐盟獲得批準,接受此類治療的患者可能還需要服用治療感染或慢性疾病的常見藥物。其中一些常規(guī)藥物會影響細胞過程,如DNA修復,進而影響治療的效果或安全性。
超過2000種藥物接受了測試
科學家們創(chuàng)建了一個全面的圖譜,展示了臨床批準的藥物如何影響人類細胞修復斷裂DNA的方式。他們測試了7000多種藥物條件,以確定每種化合物在靶向CRISPR切割后如何改變DNA修復的選擇?!拔覀冾A計該目錄將成為從事疾病建模、基因治療和腫瘤學工作的臨床醫(yī)生和研究人員的寶貴資源,”共同主要作者Philipp Kanis補充說。

圖2 DNA雙鏈斷裂修復通路調控劑的藥物篩選
發(fā)現(xiàn)DNA修復調節(jié)中的新參與者
研究小組發(fā)現(xiàn)了幾種可以影響主要修復途徑的藥物。利用篩選數(shù)據(jù),他們進一步探索了以前未被認識到的對修復結果影響最大的藥物靶點。值得注意的是,他們發(fā)現(xiàn)了之前與基因組編輯無關的兩種蛋白質在DNA修復中的新作用。這些蛋白是雌激素受體2 (ESR2)和醛氧化酶1 (AOX1)。靶向抑制ESR2可以將精確編輯的效率提高多達四倍,而抑制AOX1的藥物可以用來殺死培養(yǎng)的癌細胞,這些癌細胞缺乏一種修復途徑——這種情況適用于許多癌細胞。
該項目的高級研究員Stephan Riesenberg說:“我們的研究確定了幾種被批準的藥物,作為治療dna修復缺陷癌癥的有希望的候選藥物,提供了目前治療方法之外的潛在選擇。”“然而,我們需要進一步的研究來驗證我們從培養(yǎng)細胞實驗中獲得的發(fā)現(xiàn)是否真的能轉化為現(xiàn)實世界的醫(yī)療用途?!?/div>
參考資料
[1] Repurposing clinically safe drugs for DNA repair pathway choice in CRISPR genome editing and synthetic lethality



