摘要:本研究針對(duì)胰腺導(dǎo)管腺癌(PDAC)基質(zhì)屏障致免疫治療耐藥難題,開發(fā)了靶向FN1的LQT肽修飾LDCP納米顆粒。
在多發(fā)性骨髓瘤(Multiple Myeloma, MM)的治療領(lǐng)域,自體造血干細(xì)胞移植(ASCT)一直是關(guān)鍵的治療手段,能夠顯著提高患者的緩解深度和無進(jìn)展生存期。然而,臨床上仍面臨一個(gè)嚴(yán)峻挑戰(zhàn):部分患者在移植后早期即出現(xiàn)復(fù)發(fā),預(yù)后極差。目前,雖然國際分期系統(tǒng)(ISS)、高危細(xì)胞遺傳學(xué)異常(如del(17p)、t(4;14)等)和乳酸脫氫酶(LDH)水平等指標(biāo)已被用于風(fēng)險(xiǎn)評(píng)估,但在移植時(shí)能有效預(yù)測(cè)早期復(fù)發(fā)的生物學(xué)標(biāo)志物仍較為缺乏。
以往研究曾采用漿細(xì)胞標(biāo)記指數(shù)(PCLI)評(píng)估漿細(xì)胞增殖活性,但由于其操作繁瑣、難以推廣,臨床應(yīng)用受限。近年來,漿細(xì)胞增殖(PCPRO)檢測(cè)通過多參數(shù)流式細(xì)胞術(shù)定量骨髓中克隆性漿細(xì)胞處于S期的比例(S-phase%),為評(píng)估漿細(xì)胞增殖提供了一種更高效的方法。盡管已有研究證實(shí)診斷時(shí)S-phase%具有預(yù)后價(jià)值,但其在移植時(shí)的預(yù)測(cè)作用尚不明確。

圖1 自體干細(xì)胞移植時(shí)處于S期的殘余克隆性漿細(xì)胞對(duì)臨床結(jié)局的影響
為此,Tamer Hellou等研究人員開展了一項(xiàng)大樣本回顧性研究,旨在明確ASCT時(shí)S-phase%與患者生存結(jié)局之間的關(guān)系,并試圖識(shí)別那些可能無法從移植中獲益的高危人群,為臨床決策提供依據(jù)。該研究近期發(fā)表于《Blood Cancer Journal》。
本研究主要采用以下方法:首先,納入2013年1月至2024年8月在Mayo Clinic接受ASCT的1136例新診斷MM患者,根據(jù)移植時(shí)S-phase%分為<2%、≥2%和無法評(píng)估三組;其次,通過多參數(shù)流式細(xì)胞術(shù)(使用CD38、CD138、CD19、CD45、胞質(zhì)輕鏈κ/λ及DAPI染色)鑒定克隆性漿細(xì)胞并計(jì)算S-phase%;最后,運(yùn)用Kaplan-Meier曲線、Cox比例風(fēng)險(xiǎn)模型等統(tǒng)計(jì)方法比較各組間無進(jìn)展生存(PFS)和總生存(OS),并校正年齡、ISS分期、肌酐、細(xì)胞遺傳學(xué)風(fēng)險(xiǎn)、緩解深度及維持治療等混雜因素。
患者特征與分組
最終納入的1136例患者中,372例S-phase<2%,142例≥2%,622例因克隆性漿細(xì)胞數(shù)量不足(<300個(gè))無法評(píng)估。與S-phase<2%組相比,S-phase≥2%組患者高危細(xì)胞遺傳學(xué)異常(59.8% vs 31.9%)、ISS III期(31.6% vs 19.3%)和肌酐≥2 mg/dL(18.3% vs 8.6%)的比例均顯著更高(P<0.01),但兩組維持治療率無差異。< div="">
生存分析
中位隨訪41個(gè)月,S-phase≥2%組中位PFS為26個(gè)月,中位OS為57個(gè)月,均顯著差于S-phase<2%組(47個(gè)月和未達(dá)到)(p<0.0001)。多因素分析顯示,s-phase≥2%是pfs(hr=1.4)和os(hr=1.8)的獨(dú)立預(yù)測(cè)因子。無法評(píng)估s-phase的患者預(yù)后最佳,中位pfs達(dá)104個(gè)月,提示其代表生物學(xué)行為良好的群體。< div="">
圖1 自體干細(xì)胞移植時(shí)處于S期的殘余克隆性漿細(xì)胞對(duì)臨床結(jié)局的影響
S-phase%分層與極端高危人群
進(jìn)一步將S-phase%分為<2%、2-4.9%、5-9.9%和≥10%四個(gè)亞組后,發(fā)現(xiàn)隨著s-phase%升高,生存結(jié)局急劇惡化。s-phase≥10%的患者中位pfs僅3.5個(gè)月,中位os僅9.5個(gè)月,提示這類患者幾乎無法從asct中獲益。< div="">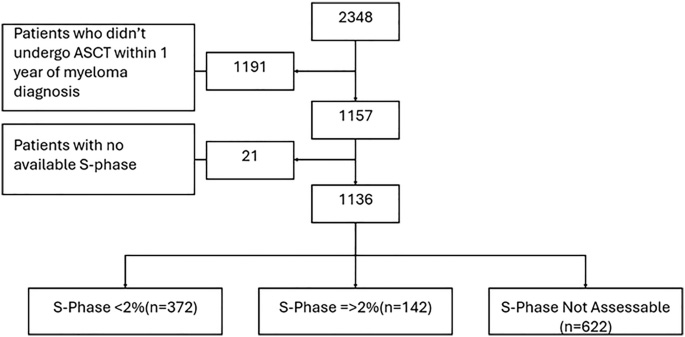
圖2 CONSORT流程圖:用于分析的患者選擇示意圖

圖2 CONSORT流程圖:用于分析的患者選擇示意圖
討論與意義
本研究首次在現(xiàn)代治療時(shí)代(含蛋白酶體抑制劑、免疫調(diào)節(jié)劑及CD38單抗誘導(dǎo)治療)背景下,證實(shí)ASCT時(shí)S-phase%是強(qiáng)效且獨(dú)立的預(yù)后標(biāo)志物。尤其值得注意的是,S-phase≥5%(特別是≥10%)的患者屬于“功能性高?!比后w,其預(yù)后極差,常規(guī)ASCT可能無法帶來臨床獲益。這一發(fā)現(xiàn)具有重要臨床意義:對(duì)于此類患者,應(yīng)考慮避免移植,轉(zhuǎn)而探索CAR-T細(xì)胞療法、雙特異性抗體等新型免疫療法作為一線治療策略。
研究的優(yōu)勢(shì)在于大樣本量和現(xiàn)代治療背景的代表性,而局限性包括回顧性設(shè)計(jì)和高S-phase%亞組樣本量較小。未來需前瞻性研究驗(yàn)證S-phase%的預(yù)測(cè)價(jià)值,并優(yōu)化高?;颊叩闹委煵呗?。
總之,該研究為MM的個(gè)體化治療提供了新思路:移植前S-phase%評(píng)估有望成為常規(guī)實(shí)踐,幫助識(shí)別那些需要替代治療策略的極端高?;颊?,最終改善臨床結(jié)局。
參考資料
[1] Stroma-Targeted Gene Delivery for Efficient Immunogene Therapy against Pancreatic Cancer
摘要:本研究針對(duì)胰腺導(dǎo)管腺癌(PDAC)基質(zhì)屏障致免疫治療耐藥難題,開發(fā)了靶向FN1的LQT肽修飾LDCP納米顆粒。
在多發(fā)性骨髓瘤(Multiple Myeloma, MM)的治療領(lǐng)域,自體造血干細(xì)胞移植(ASCT)一直是關(guān)鍵的治療手段,能夠顯著提高患者的緩解深度和無進(jìn)展生存期。然而,臨床上仍面臨一個(gè)嚴(yán)峻挑戰(zhàn):部分患者在移植后早期即出現(xiàn)復(fù)發(fā),預(yù)后極差。目前,雖然國際分期系統(tǒng)(ISS)、高危細(xì)胞遺傳學(xué)異常(如del(17p)、t(4;14)等)和乳酸脫氫酶(LDH)水平等指標(biāo)已被用于風(fēng)險(xiǎn)評(píng)估,但在移植時(shí)能有效預(yù)測(cè)早期復(fù)發(fā)的生物學(xué)標(biāo)志物仍較為缺乏。
以往研究曾采用漿細(xì)胞標(biāo)記指數(shù)(PCLI)評(píng)估漿細(xì)胞增殖活性,但由于其操作繁瑣、難以推廣,臨床應(yīng)用受限。近年來,漿細(xì)胞增殖(PCPRO)檢測(cè)通過多參數(shù)流式細(xì)胞術(shù)定量骨髓中克隆性漿細(xì)胞處于S期的比例(S-phase%),為評(píng)估漿細(xì)胞增殖提供了一種更高效的方法。盡管已有研究證實(shí)診斷時(shí)S-phase%具有預(yù)后價(jià)值,但其在移植時(shí)的預(yù)測(cè)作用尚不明確。

圖1 自體干細(xì)胞移植時(shí)處于S期的殘余克隆性漿細(xì)胞對(duì)臨床結(jié)局的影響
為此,Tamer Hellou等研究人員開展了一項(xiàng)大樣本回顧性研究,旨在明確ASCT時(shí)S-phase%與患者生存結(jié)局之間的關(guān)系,并試圖識(shí)別那些可能無法從移植中獲益的高危人群,為臨床決策提供依據(jù)。該研究近期發(fā)表于《Blood Cancer Journal》。
本研究主要采用以下方法:首先,納入2013年1月至2024年8月在Mayo Clinic接受ASCT的1136例新診斷MM患者,根據(jù)移植時(shí)S-phase%分為<2%、≥2%和無法評(píng)估三組;其次,通過多參數(shù)流式細(xì)胞術(shù)(使用CD38、CD138、CD19、CD45、胞質(zhì)輕鏈κ/λ及DAPI染色)鑒定克隆性漿細(xì)胞并計(jì)算S-phase%;最后,運(yùn)用Kaplan-Meier曲線、Cox比例風(fēng)險(xiǎn)模型等統(tǒng)計(jì)方法比較各組間無進(jìn)展生存(PFS)和總生存(OS),并校正年齡、ISS分期、肌酐、細(xì)胞遺傳學(xué)風(fēng)險(xiǎn)、緩解深度及維持治療等混雜因素。
患者特征與分組
最終納入的1136例患者中,372例S-phase<2%,142例≥2%,622例因克隆性漿細(xì)胞數(shù)量不足(<300個(gè))無法評(píng)估。與S-phase<2%組相比,S-phase≥2%組患者高危細(xì)胞遺傳學(xué)異常(59.8% vs 31.9%)、ISS III期(31.6% vs 19.3%)和肌酐≥2 mg/dL(18.3% vs 8.6%)的比例均顯著更高(P<0.01),但兩組維持治療率無差異。< div="">
生存分析
中位隨訪41個(gè)月,S-phase≥2%組中位PFS為26個(gè)月,中位OS為57個(gè)月,均顯著差于S-phase<2%組(47個(gè)月和未達(dá)到)(p<0.0001)。多因素分析顯示,s-phase≥2%是pfs(hr=1.4)和os(hr=1.8)的獨(dú)立預(yù)測(cè)因子。無法評(píng)估s-phase的患者預(yù)后最佳,中位pfs達(dá)104個(gè)月,提示其代表生物學(xué)行為良好的群體。< div="">
S-phase%分層與極端高危人群
進(jìn)一步將S-phase%分為<2%、2-4.9%、5-9.9%和≥10%四個(gè)亞組后,發(fā)現(xiàn)隨著s-phase%升高,生存結(jié)局急劇惡化。s-phase≥10%的患者中位pfs僅3.5個(gè)月,中位os僅9.5個(gè)月,提示這類患者幾乎無法從asct中獲益。< div="">
圖2 CONSORT流程圖:用于分析的患者選擇示意圖

圖2 CONSORT流程圖:用于分析的患者選擇示意圖
討論與意義
本研究首次在現(xiàn)代治療時(shí)代(含蛋白酶體抑制劑、免疫調(diào)節(jié)劑及CD38單抗誘導(dǎo)治療)背景下,證實(shí)ASCT時(shí)S-phase%是強(qiáng)效且獨(dú)立的預(yù)后標(biāo)志物。尤其值得注意的是,S-phase≥5%(特別是≥10%)的患者屬于“功能性高?!比后w,其預(yù)后極差,常規(guī)ASCT可能無法帶來臨床獲益。這一發(fā)現(xiàn)具有重要臨床意義:對(duì)于此類患者,應(yīng)考慮避免移植,轉(zhuǎn)而探索CAR-T細(xì)胞療法、雙特異性抗體等新型免疫療法作為一線治療策略。
研究的優(yōu)勢(shì)在于大樣本量和現(xiàn)代治療背景的代表性,而局限性包括回顧性設(shè)計(jì)和高S-phase%亞組樣本量較小。未來需前瞻性研究驗(yàn)證S-phase%的預(yù)測(cè)價(jià)值,并優(yōu)化高?;颊叩闹委煵呗?。
總之,該研究為MM的個(gè)體化治療提供了新思路:移植前S-phase%評(píng)估有望成為常規(guī)實(shí)踐,幫助識(shí)別那些需要替代治療策略的極端高?;颊撸罱K改善臨床結(jié)局。
參考資料
[1] Stroma-Targeted Gene Delivery for Efficient Immunogene Therapy against Pancreatic Cancer



